Établissement Porteur

Ce marché est coordonné par la filière Médicaments aux Hospices Civil de Lyon
Objet du marché
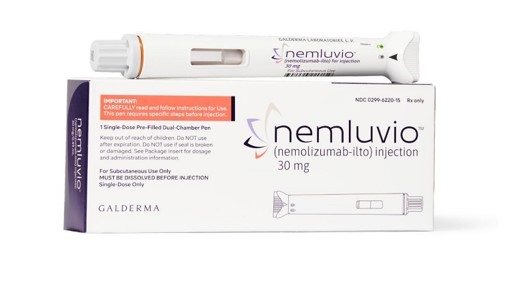
Ce marché correspond à un nouveau périmètre dans la prise en charge des patients adultes atteints de prurigo nodulaire modéré à sévère qui nécessitent un traitement systémique dans le cadre de l’autorisation d’Accès Direct. NEMLUVIO est un anticorps monoclonal administré par voie sous cutanée. NEMLUVIO a obtenu son AMM en France en février 2024.
Il se présente sous la forme d’un stylo pré rempli dosé à 30mg.
Depuis Août 2025, NEMLIVIO a obtenu une autorisation d’Accès direct.
Acteurs concernés
Pharmaciens
Valeur ajoutée achat
Proposer une solution à un besoin de santé publique. Le prurigo nodulaire est une maladie inflammatoire chronique de la peau, douloureuse et affichante. Cette pathologie peut être responsable d’une altération de la qualité de vie chez les patients les plus sévères avec un inconfort physique et un impact sur la vie sociale. Dans le cadre de prurigo nodulaire, la population cible est estimée à environ 13 000 patients en France.
Simplifier l’accès à ces traitements : Ce médicament bénéficie du dispositif d’accès direct (LFSS article 62) qui permet une mise à disposition et une prise en charge anticipée, pour un produit ayant un service médical rendu (SMR) majeur, avant l’obtention de son prix définitif. JO du 29 Aout 2025.Ce médicament va dans un premier temps être délivré par rétrocession, puis passera probablement en ville dès l’obtention de son statut en droit commun.
La prescription est réservée aux spécialistes en allergologie, en dermatologie, en médecine interne ou en pédiatrie. Ce médicament nécessite une surveillance particulière. L’ordonnance doit comporter la mention « prescription au titre de l’accès direct ».
Les points forts
Mise à disposition immédiate d’une nouvelle spécialité
Simplification de l’accès
Premier marché national, absence de marchés régionaux au démarrage du marché UniHA
Souveraineté : Fabrication en Suède et en France
Innovation :
- Traitement innovant pour le prurigo nodulaire modéré à sévère, administré par voie sous cutanée via un anticorps monoclonal.
- Première spécialité disponible sur le marché national pour cette pathologie
Accompagnement
Le statut du médicament sera révisé dans un an maximum, et son prix sera déterminé par le CEPS, avec remboursement des sommes perçues en plus par le fournisseur.
Lors de la détermination du prix CEPS, aider les adhérents à obtenir le remboursement de l’écart de prix.